BJN#211 – Un « mab » dans l’IRC
Cette BJN est rédigée en rapport avec la référence bibliographique suivante :
Ridker PM, Devalaraja M, Baeres FMM, Engelmann MDM, Hovingh GK, Ivkovic M, Lo L, Kling D, Pergola P, Raj D, Libby P, Davidson M; RESCUE Investigators. IL-6 inhibition with ziltivekimab in patients at high atherosclerotic risk (RESCUE): a double-blind, randomised, placebo-controlled, phase 2 trial. Lancet. 2021 May 29;397(10289):2060-2069.
Lien vers l’article : IL-6 inhibition with ziltivekimab in patients at high atherosclerotic risk (RESCUE): a double-blind, randomised, placebo-controlled, phase 2 trial
Merci à Antoine Braconnier, Néphrologue à Reims, membre du Comité Scientifique du CJN, pour cette synthèse bibliographique. Vous aussi, n’hésitez pas à nous envoyer vos lectures !
Introduction
L’inhibition de l’inflammation ciblant l’inflammasome NLRP3 via la voie de l’IL-1 et de l’IL-6 est une méthode émergente pour le traitement et la prévention de l’athérosclérose. L’étude « Canakinumab Anti-Inflammatory Thrombosis Outcomes Study » (CANTOS) en utilisant l’inhibition de l’IL-1β et deux essais sur la colchicine (qui pourrait indirectement inhiber la fonction de NLRP) en sont les principales preuves (Essais LODOCO2 et COLCOT).
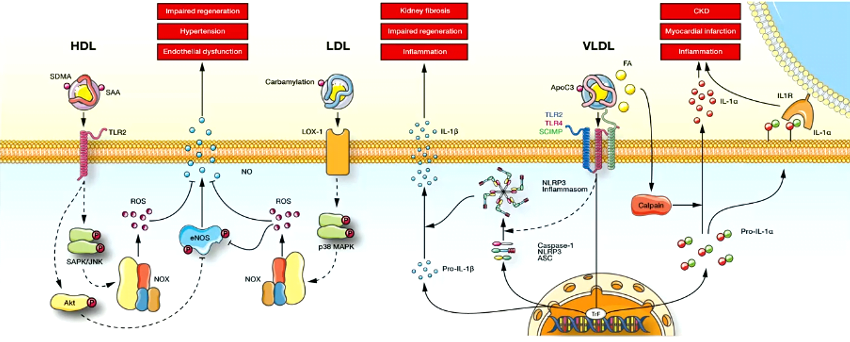
D’après Schunk et al. Circulation 2021 Jul 1, par Speer ERA-EDTA 2021
Dans ces études, l’inhibition de l’IL-6 réduisait le taux de CRP. Dans l’essai CANTOS, l’ampleur de la prévention de l’athérosclérose associée au canakinumab était proportionnelle à la réduction des taux d’IL-6 et de CRP. Un essai récent de réduction de l’inflammation utilisant du méthotrexate à faible dose ne réduisait pas l’IL-6 et les événements vasculaires, suggérait que les anti-inflammatoires ne réduisant pas l’IL-6 étaient peu susceptibles d’être efficaces sur l’athéroprotection. On sait depuis longtemps que les taux d’IL-6 permettent de prédirent les événements vasculaires en prévention primaire et secondaire. Contrairement à la CRP, des études suggèrent que l’IL-6 est susceptible d’être un facteur causal d’athérosclérose.
Patients/matériels et méthodes
Sur la base de ces données, les auteurs ont émis l’hypothèse qu’un ciblage direct de l’IL-6 pourrait optimiser le bénéfice athérosclérotique chez des personnes à haut risque d’athérosclérose. Le ziltivekimab, un anticorps monoclonal humain ciblant le ligand de l’IL-6 humain, a été développé spécifiquement pour le traitement de l’athérosclérose. En tant qu’anticorps monoclonal ciblant le ligand de l’IL-6 plutôt que le récepteur de l’IL-6, le ziltivekimab est utilisé à de plus faibles dose et pourrait avoir moins d’effets indésirables (toxicité hématologique et hépatique en particulier) que les autres molécules (tocilizumab, sarilumab).
L’essai RESCUE (n = 264) est un essai de phase 2 qui évalue les effets du ziltivekimab administré mensuellement en SC et à différents dosages (placebo, 7.5 mg, 15 mg, 30 mg) dans une population souffrant de maladie rénale chronique stade 3- 4et présentant un risque cardiovasculaire élevé avec un taux élevé de CRPus (> 2 mg/L)
Résultats
12 semaines après la randomisation le ziltivekimab a réduit de façon marquée les biomarqueurs de l’inflammation (CRP us) comparativement au placebo
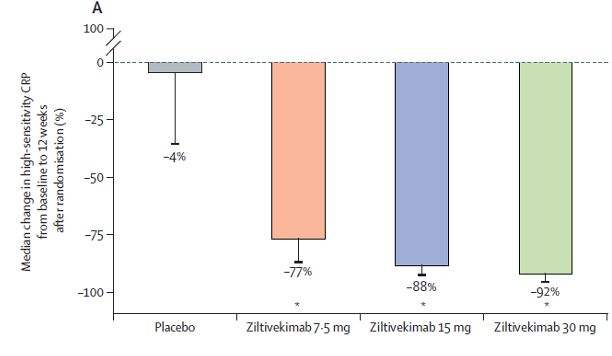
Des résultats similaires ont été mis en évidence sur les biomarqueurs de la thrombose liés à l’athérosclérose (fibrinogène, sérum amyloïde A, haptoglobine, phospholipase A2 sécrétoire, lipoprotéine(a))
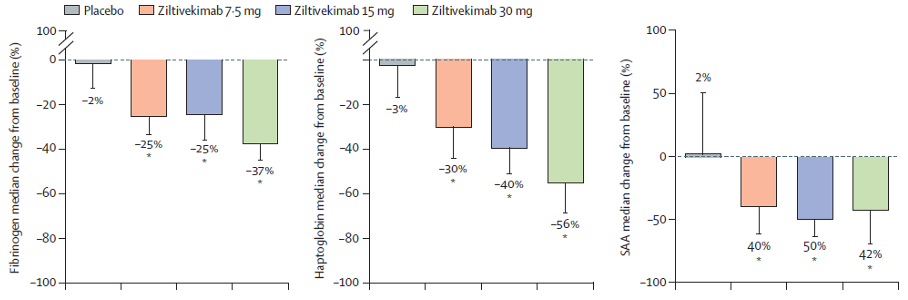
Le ziltivekimab a été bien toléré, n’a pas modifié le rapport cholestérol total/cholestérol HDL et n’a entraîné aucune réaction grave.
Conclusion
Sur la base de ces données, un essai de phase 3 (ZEUS) va débuter en 2021. Il doit inclure 6200 patients atteint d’une IRC stade 3-4 avec une CRPus ≥ 2mg/L. Il comparera une injection de ziltivekimab mensuelle versus placebo. Le critère de jugement principal est l’apparition de MACE
Références
- Ridker PM, Everett BM, Thuren T, et al. Antiinflammatory therapy with canakinumab for atherosclerotic disease. N Engl J Med 2017; 377: 1119–31.
- Tardif JC, Kouz S, Waters DD, et al. Efficacy and safety of low-dose colchicine after myocardial infarction. N Engl J Med 2019; 381: 2497–505.
- Nidorf SM, Fiolet ATL, Mosterd A, et al. Colchicine in patients with chronic coronary disease. N Engl J Med 2020; 383: 1838–47.