BJN#268 – L’utilisation de la spironolactone chez les patients MRC n’est pas une mince affaire
Merci à Valentin Maisons, CCA au CHU de Tours,
N’hésitez pas, si vous le souhaitez, à nous envoyer vos lectures !
Cette BJN est rédigée en rapport avec cet article :
Low-dose spironolactone and cardiovascular outcomes in moderate stage chronic kidney disease: a randomized controlled trial, publié par Hobbs et al. dans Nature Medecine en 2024.
Introduction
La maladie rénale chronique (MRC) de stade 3b est associée à un risque élevé de progression vers l’insuffisance rénale terminale et de complications cardiovasculaires. Malgré l’efficacité démontrée des inhibiteurs de l’enzyme de conversion (IEC) et des antagonistes des récepteurs de l’angiotensine II (ARA-II), le risque cardiovasculaire demeure élevé chez ces patients. Le blocage des récepteurs minéralocorticoïdes avec des antagonistes stéroïdiens comme la spironolactone pourrait offrir des bénéfices cardiovasculaires supplémentaires (y compris par rapport aux antagonistes non stéroïdiens comme la finérénone), mais l’utilisation de cette molécule chez les patients atteints de MRC modérée suscite des inquiétudes liées aux effets secondaires.
Matériels et méthodes
Cette étude randomisée ouverte avec évaluation des critères de jugement en aveugle (PROBE) a inclus 1 434 adultes âgés en moyenne de 74,8 ans, atteints de MRC stade 3b. Cela représentait seulement 45 % de l’effectif prévu initialement après calcul du nombre de sujets nécessaires. Les patients ont été répartis 1 : 1 pour recevoir soit une faible dose de spironolactone (25 mg/jour) en plus des soins habituels, soit uniquement les soins habituels. Le critère principal évaluait la survenue de décès, d’hospitalisation pour maladies cardiaques, accidents vasculaires cérébraux, insuffisance cardiaque, accidents ischémiques transitoires ou maladie artérielle périphérique.
Résultats
Après 3 ans de suivi, aucune différence significative n’a été observée entre les deux groupes concernant le critère principal composite (HR=1,05; IC95% [0,81-1,37]). Les deux tiers des participants randomisés dans le groupe spironolactone ont arrêté le traitement dans les 6 mois. La plupart arrêtaient parce qu’ils répondaient aux critères d’arrêt de sécurité pré-spécifiés, avec en chef de fil la baisse du DFG (n = 239, 35.4%) ou l’hyperkaliémie (n = 54, 8.0%). L’hyperkaliémie était plus fréquente chez les patients sous spironolactone (24,7 % contre 13,4 % dans le groupe contrôle, p<0,001). Ces hyperkaliémies étaient modérées dans la majorité des cas.
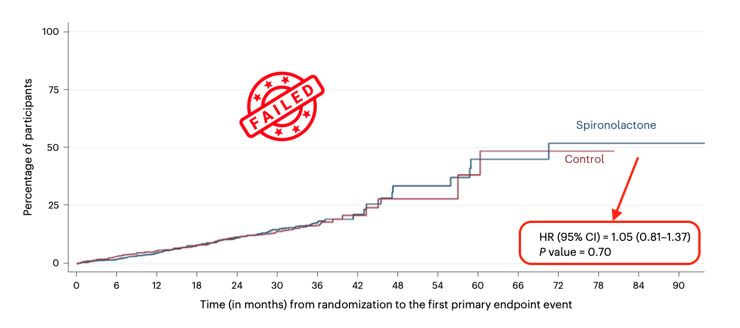
Conclusion
Chez des patients âgés atteints de MRC 3b suivis en soins primaires, l’ajout de spironolactone 25 mg/j n’a pas réduit les évènements cardiovasculaires sur 3 ans, dans un essai sous‑dimensionné où 2/3 des participants ont interrompu le traitement avant 6 mois pour des raisons de sécurité, principalement une baisse du DFG ou des hyperkaliémies. Cette étude montre principalement la mauvaise tolérance des antagonistes stéroïdiens dans cette population et donc son application difficile en pratique clinique. Cette question méritera d’être explorée à l’avenir avec l’arrivée de nouveaux chélateurs du potassium.
Les plus du papier
- Essai randomisé multicentrique de grande taille conçu selon les critères PROBE.
- Critères de sécurité clairement définis et bien surveillés.
- Importante cohorte représentative d’une population âgée typique en soins primaires.
- Analyse méthodologique assez exhaustive ; sous-groupes, analyse de sensibilité, analyses post-hoc avec étude de simulation, analyse médico-économique…
Les critiques
- Le taux élevé d’arrêt du traitement (près de deux tiers avant 6 mois) limite la capacité d’évaluer pleinement l’efficacité à long terme de la spironolactone.
- Incapacité à atteindre l’objectif initial de recrutement : seulement 45 % de l’effectif prévu.
- Données manquantes lors du suivi, notamment biologies sanguines, du fait d’un essai réalisé pendant la pandémie de COVID19.
- Pas de standardisation de la prise en charge de l’insuffisance cardiaque ou de l’hypertension artérielle (encouragement pour l’HTA à suivre les guidelines « NICE »).
- Quasi absence de co-prescriptions d’inhibiteurs de SGLT2 du fait de l’ancienneté de l’étude.
- Absence de placebo et par conséquent essai en ouvert.