BJN#191 –Le Daratumumab pour l’ABMR chronique actif, ça match ou next ?
Cette BJN est rédigée en rapport avec la référence bibliographique suivante :
Doberer K, Kläger J, Gualdoni GA, Mayer KA, Eskandary F, Farkash EA, Agis H, Reiter T, Reindl-Schwaighofer R, Wahrmann M, Cohen G, Haslacher H, Bond G, Simonitsch-Klupp I, Halloran PF, Böhmig GA. CD38 Antibody Daratumumab for the Treatment of Chronic Active Antibody-mediated Kidney Allograft Rejection. Transplantation. 2021 Feb 1;105(2):451-457.
Lien vers l’article : CD38 Antibody Daratumumab for the Treatment of Chronic Active Antibody-mediated Kidney Allograft Rejection
Merci à Maïté Meunier, Néphrologue à Toulon, membre du Comité Scientifique du CJN, pour cette synthèse bibliographique. Vous aussi, n’hésitez pas à nous envoyer vos lectures !
Introduction
Le rejet médié par les anticorps (ABMR) chronique actif est une cause de perte de fonction du transplant. Les derniers traitements étudiés (inhibiteurs du protéasome (bortezomib), anticorps anti C5, IgIV, rituximab) n’ont pas montré d’efficacité malgré des études observationnelles multiples initialement prometteuses. Les plasmocytes et les cellules natural killer (NK) sont des cibles thérapeutiques intéressantes et expriment CD38+. Or CD38 + fait l’objet d’une thérapie ciblée dans le cadre du myélome multiple.
Patients/matériels et méthodes
Il s’agit d’un rapport de cas d’un patient âgé de 49 ans transplanté rénal depuis 13 ans avec un diagnostic concomitant d’un myélome multiple et d’un ABMR chronique actif. L’anticorps monoclonal anti CD38 (Daratumumab) en intraveineux qui était indiqué pour le myélome a été administré pendant 9 mois selon le protocole : 16 mg/kg hebdomadaire pendant 8 semaines, puis bimensuel pendant 4 mois puis mensuel, avec une prémédication par dexamethasone 20mg.
La production in vitro d’alloanticorps par les cellules de la moelle du patient était étudiée via une purification de cellules CD138+ mises en culture et une analyse du surnageant.
Le suivi du patient était de 1 an et incluait le suivi des Ac anti-HLA en single antigen, le phénotypage des cellules circulantes sanguines, un myélogramme et une biopsie rénale à M3 et M9, avec analyse sur la biopsie des profils d’expression moléculaire en lien avec le rejet via le « Molecular Microscope Diagnostic System (MMDx) » afin de définir des archétypes interprétés en analyse de composé principal.
Résultats
Le patient était immunisé DSA de classe II (DQB1*06:02; MFI: 3761), la biopsie du transplant était indiquée par une insuffisance rénale aigue et une protéinurie et retrouvait : g2 cpt1 cg3 C4D0 i0 t0 IFTA 1 i-IFTA 1, sans atteinte du myélome associée à la biopsie du transplant (IF chaines lambda négatives notamment). Le patient a poursuivi son traitement immunosuppresseur qui était constitué de tacrolimus (taux cibles avant le diagnostic de rejet 5-8 ng/ml versus 7-10 ng/ml après), d’acide mycophenolique (1440 mg/jour avec une réduction à 360 mg/jour à M7 après le diagnostic de rejet à cause de diarrhées) et de prednisolone 5mg/jour.
Le Daratumumab a permis une déplétion persistante des cellules CD138+ dans la moelle et le sang, ainsi que les cellules NK dans le sang et le greffon. En même temps les DSA sériques ont disparu en 14 semaines, ainsi que la production in vitro d’alloanticorps par les cellules CD138+ issus de la moelle du patient.
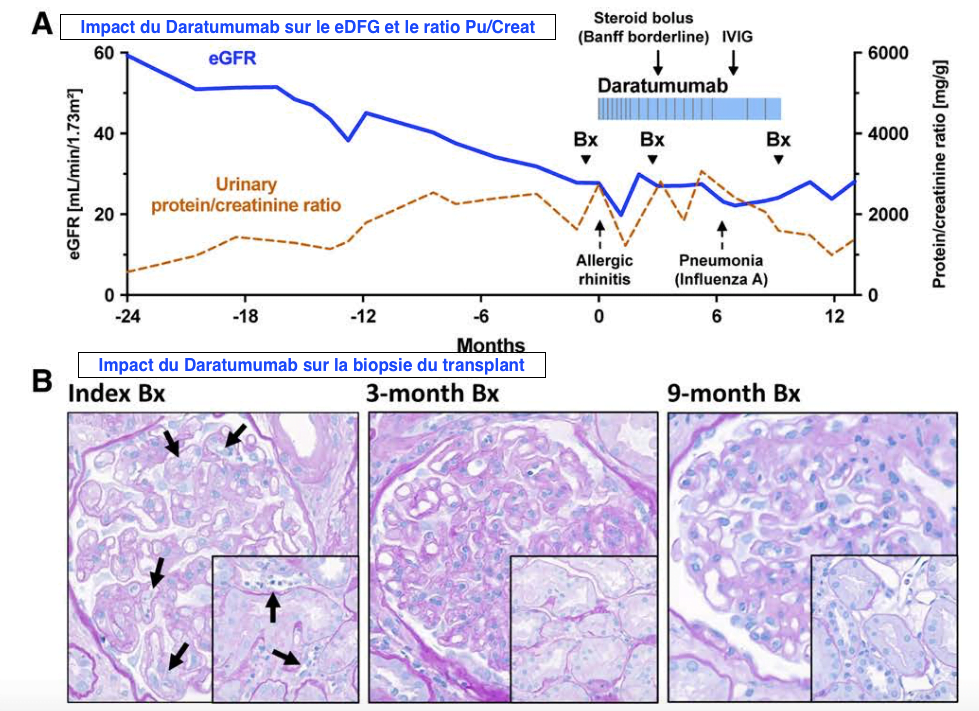
La biopsie du transplant rénal à 3 mois a montré une résolution de l’inflammation de la microcirculation (g+cpt) ainsi que de la signature moléculaire d’activité humorale, via « l ’AMR score » qui est passé de 0,79 à 0,2. La même biopsie montrait une inflammation tubulointerstitielle infraclinique traitée par stéroïdes (i1t3) avec une persistance des doubles contours (cg3).
Le suivi a été de 1 an avec une stabilité de la fonction rénale. La pente du eDFG était de −15.44 mL/min/1.73 m2/an les 2 dernières années avant le traitement, puis de +0.73 mL/min/1.73 m2 lors des 12 mois de suivi, le ratio kappa lambda s’est normalisé. La tolérance du traitement a été marquée par une rhinite allergique à la première perfusion et une pneumopathie virale grippe A positive à 6 mois.
 Conclusion
Conclusion
Cibler les cellules CD38+ pour induire une déplétion de plasmocytes et de cellules NK pourrait être une stratégie pour contrer le rejet humoral chronique actif. Cette étude encourage la réalisation d’essais contrôlés randomisés pour clarifier le rôle du daratumumab en transplantation rénale.
Les plus du papier
- Molécule prometteuse
- Suivi par biopsie du transplant rénal
- Signature moléculaire du rejet
Les critiques
- Il s’agit d’un rapport de cas
- Nécessité d’études complémentaires plus robustes pour pouvoir conclure
- Échecs antérieurs de molécules également prometteuses
- Risque infectieux majoré
- Discordance entre le score moléculaire de rejet cellulaire qui est resté négatif sur la biopsie à M3 et le diagnostic anatomopathologique de rejet borderline selon la classification de Banff 2017.